에이즈 완치 환자, 유전자 교정 치료의 가능성을 열다
강의 준비를 위해 자료를 검색하던 중, 세계 최초 에이즈 완치 환자 티모시 레이 브라운(Timothy Ray Brown)이 2020년 9월 사망했다는 뉴스를 보았습니다. ‘베를린 환자(The Berlin patient)’로 알려진 그는 독일 유학 중 HIV에 감염됐고 설상가상으로 백혈병까지 진단받았습니다. 이를 치료하기 위해 2007년 조혈모세포 이식을 받았는데 운이 좋게도 공여자가 HIV 감염에 대한 저항성을 갖고 있었습니다. HIV의 침입을 막을 수 있는 특정 유전자 변이가 자연적으로 존재했던 것이죠. 이 덕분에 브라운은 HIV로부터 완전히 치유됐지만 끝내 백혈병이 재발했습니다. 자신의 경험을 바탕으로 에이즈 치료법 연구를 적극적으로 지지했던 브라운의 죽음에 많은 사람들이 애도했습니다.
HIV는 면역세포인 T세포의 막 표면에 존재하는 수용체를 통해 감염을 일으키는데, 이 수용체를 구성하는 단백질 중 하나가 CCR5 유전자에 의해 발현됩니다. 브라운이 이식받은 조혈모세포는 정상적인 CCR5 유전자 대신 32개의 염기서열이 사라진 ‘돌연변이 CCR5 유전자(CCR5-Δ32)’만을 갖고 있었습니다. 이로 인해 HIV에 의한 T세포 감염이 일어나지 않아 에이즈로부터 안전했던 것입니다.
유전자편집 기술의 발전과 윤리적 문제
브라운의 사례를 바탕으로 연구자들은 인공적으로 CCR5 유전자에 돌연변이를 유도해 HIV 감염을 극복하는 연구에 집중했습니다. 환자의 조혈모세포를 분리해 CCR5 유전자에 HIV 저항성을 갖는 돌연변이를 유도한 뒤 이를 다시 이식하는 방식이, 유전적으로 전혀 다른 기증자의 조혈모세포를 이식하는 것보다 훨씬 바람직하기 때문입니다. 이를 위해 1세대 유전자가위인 ‘징크핑거 뉴클레이즈Zinc-Finger Nuclease, ZFN’가 연구에 활발히 활용됐습니다. 하지만 초기 유전자가위는 한계가 뚜렷했습니다. 엉뚱한 유전자를 잘라내는 오프타깃(off-target) 현상이 발생했고 과도한 DNA 손상 때문에 세포 독성이 매우 강했습니다. 게다가 인간 유전자 중에는 CCR5와 염기서열이 매우 유사한 CCR2와 같은 유전자도 있는데, ZFN은 이들을 정확히 구분하지 못하는 경우도 많았죠. 이러한 한계는 2세대 유전자가위 ‘탈렌Transcription Activator-Like Effector Nuclease, TALEN’이 개발되며 많이 해결됐습니다.
2012년에는 3세대 유전자가위 ‘CRISPR-Cas9(이하 크리스퍼)’이 개발됐습니다. 박테리아가 침입하는 바이러스(박테리오파지)나 플라스미드와 같은 외래 유전물질을 정교하게 파괴하도록 진화된 Cas9 단백질을 이용해 원하는 DNA 염기서열만을 선택해 절단할 수 있게 됐습니다. 이 기술을 최초로 규명한 에마뉘엘 샤르팡티에(Emmanuelle Charpentier)와 제니퍼 다우드나(Jennifer A. Doudna)는 2020년 노벨화학상을 수상했습니다. 완벽하진 않더라도, 크리스퍼 유전자가위를 이용해 CCR5 유전자를 원하는 방향으로 교정할 수 있다는 것이 널리 인정받게 됐습니다.
2018년 11월, 중국 남방과학기술대 허젠쿠이(賀建奎) 박사는 크리스퍼 유전자가위로 인간 배아의 CCR5 유전자를 편집해 HIV에 저항성을 가진 쌍둥이가 태어났다고 발표해 큰 논란을 일으켰습니다. 수정란은 HIV에 감염된 부모로부터 기증받은 것이었지만 중국 법원은 이를 불법 의료행위로 판단해 그에게 징역 3년과 벌금 300만 위안(약 5억 원)을 선고했습니다. 인간의 게놈을 인위적으로 편집해 이전과 다른 인류를 만들어낼 수 있다는 점에서, 인간 배아를 대상으로 한 유전자 편집은 여전히 큰 윤리적 논쟁을 안고 있습니다.
여담으로 2024년 다국적 제약사 길리어드는 미국 FDA로부터 HIV 치료제 ‘선렌카(레나카파비르)’ 승인을 받았습니다. 이 약물은 HIV에 감염된 세포가 바이러스를 복제할 때 그 외벽을 형성하는 캡시드 단백질을 비활성화해 바이러스의 증식을 억제합니다. 임상시험에서 HIV 감염에 취약한 대상자들에게 6개월 간격으로 2년간 주사한 결과 감염이 거의 완벽하게 차단되는 효과가 확인됐습니다. 선렌카의 효능과 작용에 대한 추가 연구와 임상 결과가 매우 기대됩니다.
개인 맞춤형 유전자 교정 치료, 현실이 되다
유전자 편집 기술은 크리스퍼 유전자가위의 등장 이후에도 계속 발전하고 있고, 불치병으로 여겨지던 희귀난치성 유전질환의 치료에도 새로운 가능성이 열리고 있습니다. 최근에는 DNA를 절단하지 않고 특정 염기만 정밀하게 바꿀 수 있는 염기편집기(Base editor)와 원하는 염기서열을 정교하게 삽입할 수 있는 프라임편집기(Prime editor)가 등장하면서 안전성과 정확도가 크게 향상됐습니다. 실제로 많은 연구에서 기존 크리스퍼 방식보다 세포 손상이 적고 더 정교한 유전자 교정이 가능하다는 결과가 보고되고 있습니다.
▲염기편집기를 이용해 희귀난치성 질환을 갖고 태어난 Baby KJ
지난해에는 염기편집기를 이용해 희귀난치성 질환을 갖고 태어난 아기를 치료한 사례가 보고됐습니다. 이는 환자에게 적용된 최초의 개인맞춤형 유전자 편집 치료 사례입니다. ‘Baby KJ’로 알려진 이 아이는 요소회로 대사이상증인 CPS1Carbamoyl Phosphate Synthetase1, 카르바모일 인산 합성효소1 결핍증을 갖고 태어났습니다. 우리 병원 의학유전학센터에 따르면 8만 명당 1명꼴로 발생하는 희귀질환입니다. CPS1 결핍으로 인해 혈액에 암모니아 수치가 지나치게 높아지면 신경계에 치명적인 영향을 미쳐 발작이나 혼수상태 등으로 이어질 수 있습니다.
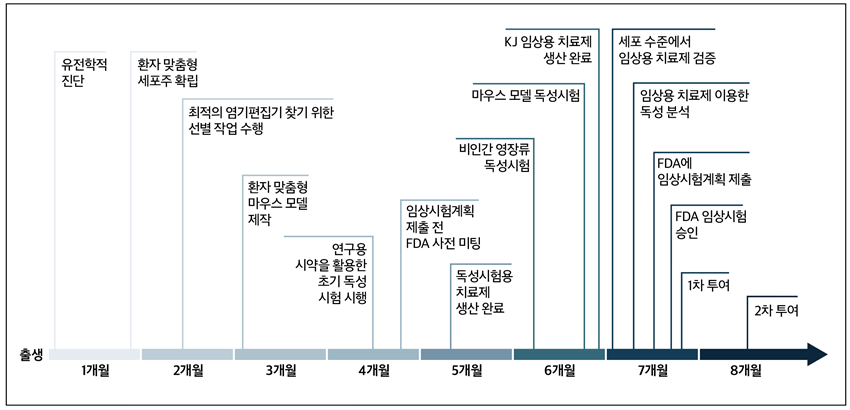
▲ Baby KJ의 치료 타임라인
위 그림이 보여주듯 치료는 매우 신속하게 진행됐습니다. 출생 후 며칠 만에 CPS1 결핍증 진단을 받았고, 한 달도 되기 전에 환자 유래 세포주Cell Line, 체외에서 지속적으로 증식하도록 만들어진 세포가 확립되었습니다. 이 세포주를 이용한 실험을 통해 Baby KJ의 돌연변이를 교정할 수 있는 최적의 염기편집기를 한 달 반 만에 알아냈습니다. 하지만 세포주는 매우 단순한 시스템이기 때문에 고도로 복잡한 체내에서는 어떤 독성이 나타날지 예측할 수 없었죠. 이에 Baby KJ와 동일한 돌연변이 염기서열을 가진 형질전환 마우스를 제작한 뒤 초기 독성시험과 영장류 독성시험까지 빠르게 진행했습니다. 동시에 FDA와의 협의를 거쳐 임상시험 승인을 받았고 첫 치료제 투여가 이뤄졌습니다. 출생부터 치료 종료까지 8개월이 채 걸리지 않았습니다.
Baby KJ는 다행히 좋은 치료 효과를 얻었고, 심각한 부작용도 나타나지 않았습니다. Baby KJ의 치료 사례는 개인 맞춤형 유전자 교정 치료가 유전질환을 갖고 태어날 수 있는 많은 아기들에게 건강한 삶을 새롭게 선물할 수 있을 것이라는 희망을 보여줍니다.













