▶ <유전자 교정, 불치의 한계를 넘어 새 삶을 선물하다> 에서 이어짐
크리스퍼 유전자가위로 만든 최초의 유전자 교정 치료제
환자 치료를 위해 승인된 세계 첫 유전자 교정 치료제는 ‘카스게비(CASGEVY)’입니다. 수혈의존성 베타 지중해빈혈(TDT)과 낫세포빈혈증(SCD) 치료를 위해 크리스퍼 테라퓨틱스크리스퍼 유전자가위 기술로 2020년 노벨 화학상을 받은 에마뉘엘 샤르팡티에 등이 창업와 버텍스 파마슈티컬이 공동 개발했습니다. TDT와 SCD는 모두 헤모글로빈을 구성하는 단백질을 암호화하는 유전자인 베타글로빈(β-globin)에 생긴 돌연변이로 인해 발생합니다. TDT의 경우 베타글로빈 합성이 크게 감소하거나 완전히 소실되고, SCD는 적혈구의 변형과 이로 인한 심각한 혈관 막힘, 용혈 현상이 일어나게 됩니다.
앞서 소개한 1편에서는 태어날 때부터 보유하고 있는 돌연변이를 직접 교정하거나 돌연변이 유전자를 아예 없애는 방식의 유전자 교정 치료를 이야기했지만, 이번 글에서 소개할 카스게비는 완전히 다른 방식으로 작동합니다. 바로 돌연변이를 상쇄할 수 있는 ‘다른 유전자’의 발현을 늘리는 것입니다. 이를 설명하려 하니 저의 오래전 기억이 떠오릅니다.
녹아웃 마우스유전자를 인공적으로 파괴해 비활성화시킨 유전자 변형 마우스의 태반조직에서 태아의 혈관을 관찰해야 했는데, 엄마의 혈관과 태아 유래 혈관을 어떻게 구별해야 하는지 몰라 매우 난감했습니다. 문제는 생각보다 쉽게 풀렸습니다. 바로 적혈구의 모양이 달랐던 것입니다. 엄마의 적혈구는 우리가 잘 알고 있듯 핵이 없고 가운데가 패인 원반 모양입니다. 이에 비해 태아 유래 적혈구는 핵이 있고 크기가 훨씬 큽니다. 또 다른 차이는 적혈구 속 헤모글로빈의 구성입니다. 태아 시기에는 각각 2개의 알파글로빈과 감마글로빈 단백질로 구성(α2γ2)되어 있다가, 태어난 후에는 감마글로빈의 발현이 억제되고 베타글로빈으로 대체되어 α2β2 형태의 헤모글로빈을 형성하는 것이었습니다.
연구자들은 감마글로빈이 베타글로빈으로 대체되는 이유를 추적한 끝에 ‘BCL11A’라는 단백질이 감마글로빈의 특정 염기서열에 결합해 감마글로빈의 발현을 억제한다는 것을 알아냈습니다. 따라서 BCL11A가 발현되지 못하게 하면 감마글로빈이 정상적으로 발현되고, 베타글로빈의 돌연변이로 인해 생기는 질병을 치료할 수 있을 것이라는 가설이 받아들여졌습니다. 하지만 BCL11A는 면역세포 생성에 필수적인 요소였고, 태어날 때부터 이 유전자가 결핍된 마우스는 출생 직후 사망하는 문제가 있었습니다. 적혈구 형성 외에도 매우 중요한 역할을 하기 때문에 함부로 없앨 수 없는 것이었죠.
그렇다면 BCL11A가 ‘적혈구가 생성되는 동안에만’ 사라진다면 어떨까요? 연구자들은 조혈모세포로부터 적혈구로 분화되는 세포에서만 BCL11A를 활성화시키는 염기서열인 ‘BCL11A 유전자의 적혈구계 인핸서(BCL11A Erythroid enhancer)’를 발견했습니다. 이 인핸서는 적혈구로 분화되지 않는 다른 세포들에서는 작동하지 않았습니다. 즉 이 인핸서만 제거하면 전체 면역 체계에는 영향을 주지 않으면서 오직 적혈구에서만 BCL11A 단백질 생성을 차단해 감마글로빈이 발현되도록 유도할 수 있는 것이죠. 따라서 환자의 조혈모세포를 추출한 뒤 이 인핸서를 없애고 다시 주입하면, 감마글로빈이 발현되는 건강한 적혈구가 생성됩니다. 환자의 조혈모세포에서 이 인핸서만 정밀하게 파괴할 수 있는 크리스퍼 유전자가위가 개발됐고, 그렇게 BCL11A 적혈구계 인핸서가 제거된 조혈모세포를 치료제로 개발한 것이 바로 카스게비인 것입니다.
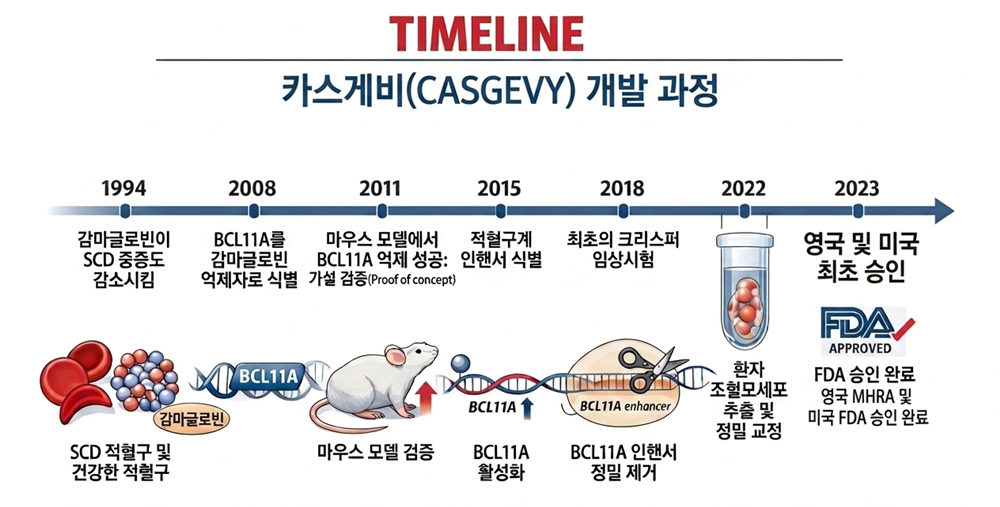
하지만 아무리 환자 유래 조혈모세포라고 해도 유전자가 교정된 이상 치료제를 환자에게 사용하기 위해서는 실험동물을 이용한 전임상시험을 반드시 거쳐야 합니다. 이때 ‘NBSGW’라는 특별한 형질전환 마우스 모델이 사용됐습니다. 이 마우스 모델이 특별한 이유는 대부분의 면역시스템이 파괴돼 있어 이식된 인간 유래 세포가 잘 증식할 수 있고, 특히 인간의 조혈모세포가 잘 안착할 수 있는 유전자 구성을 갖고 있기 때문입니다. 연구진은 카스게비를 투여한 뒤 적혈구가 분화되는 동안 BCL11A 단백질이 감소하고 감마글로빈의 발현이 점차적으로 증가함을 확인했습니다. 이러한 긍정적인 전임상시험 결과를 바탕으로 2018년부터 임상시험에 본격 돌입했습니다. 결과는 놀라웠습니다. 생존을 위해 정기적으로 수혈을 받아야만 했던 TDT 환자 42명 중 39명은 최소 1년 이상 수혈을 받지 않아도 될 정도로 효과가 좋았던 것입니다. 이러한 성공적인 결과를 바탕으로 카스게비는 2023년 말 영국과 미국 정부로부터 공식적인 치료제로 인정받게 되었습니다.
탄탄한 기초연구가 이뤄낸 성과
수십 년간의 헤모글로빈 발현 기초연구에 기반한 가설, 크리스퍼 유전자가위 기술, 그리고 5년간의 임상시험까지. 저는 이 지난한 과정을 거쳐 탄생한 카스게비가 ‘세계 최초 유전자 교정 치료제’라는 사실 외에도 특별한 이유가 있다고 생각합니다.
보통 유전자 교정 치료제를 개발하려면 어떤 유전 변이를 고칠지 먼저 결정해야 합니다. 일반인과 구별되는 환자만의 유전자 변이를 찾고 이를 마우스 게놈에 복사해 환자와 동일한 질병이 발현되는지 확인해야 합니다. 환자를 모사한 마우스에서 질병이 발생한다면 이는 질병 기전 연구뿐 아니라 신약의 유효성과 안전성을 검증하는 질환 동물 모델로서 매우 중요하게 사용됩니다. 방대한 시간과 비용을 들여 이 과정을 거치는 이유는 동일한 유전자에도 수많은 변이가 존재할 수 있으며, 이들 중에는 병을 일으키는 것도 있는 반면 그렇지 않은 것도 부지기수이기 때문입니다. 이렇게 검증된 특정 돌연변이를 정상으로 되돌리거나 파괴하는 것이 유전자 교정 치료의 일반적인 접근 방식입니다.
하지만 카스게비는 달랐습니다. 유전자 변이를 일일이 찾아 교정하는 방식 대신, 기초연구를 통해 밝혀진 과학적 사실과 질병의 근본 원리를 바탕으로 적혈구가 만들어지는 동안에만 BCL11A 유전자가 발현되지 않도록 설계됐죠. 덕분에 베타글로빈 유전자에 어떤 종류의 변이가 있든(SCD든 TDT든 관계없이) 치료할 수 있습니다. 기초연구의 힘과 중요성을 가장 잘 보여준 사례가 아닐까 생각하는 이유입니다. 마침 BCL11A 유전자의 적혈구계 인핸서를 규명한 연구자들이 최근 ‘과학 오스카상’ 또는 ‘실리콘벨리 노밸상’으로 불리는 브레이크스루상(Breakthrough Prize) 수상자로 선정됐습니다. 기초과학이 연구에 머물지 않고 불치의 한계를 넘어 거대한 혁신으로 이어진다는 점을 전 세계가 인정한 것이라 더욱 뜻깊습니다.
유전자 교정 치료제의 개발 외에도 기초연구는 질병의 이해와 진단, 그리고 새로운 치료법 개발 등 다양한 측면에서 긍정적인 영향을 줍니다. 많은 연구자들이 어려운 여건 속에서도 꾸준히 기초연구를 수행하기 위해 애쓰고 있습니다. 시간과 노력이 필요하겠지만, 이 연구로 인해 혜택을 받을 환자들을 상상하며 더욱 연구에 매진하기를 진심으로 응원합니다.














